Образование мицеллСтраница 1
Рассмотрим, что происходит при растворении углеводородов с длинной цепью в воде. Из-за весьма неблагоприятных "гидрофобных" взаимодействий, описанных в - предыдущем разделе, их растворимость будет очень мала. Такие углеводороды, как додекан, смогут растворяться в воде лишь до определенной концентрации, а выше этой концентрации они будут образовывать отдельную фазу. При дальнейшем добавлении до декана будет просто увеличиваться содержание додекановой фазы, а концентрация додека-на, растворенного в воде, не изменится.
Посмотрим теперь, что произойдет при попадании в воду амфи-фильной молекулы, например додецилсульфата натрия. Молекула этого типичного детергента состоит из неполярной части и из сильно заряженной полярной группы, расположенной на одном из концов цепи. Когда достигается предел растворимости мономерной формы этого детергента, он также образует отдельную фазу. Однако в данном случае эта "фаза" диспергирована в виде небольших агрегатов, называемых мицеллами, по всему объему воды.
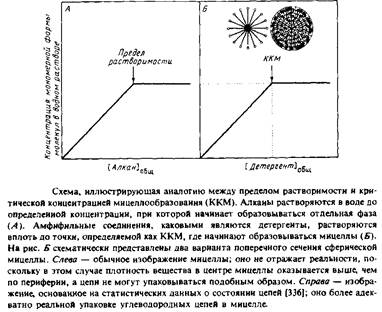
Поскольку взаимодействия между полярной головкой и водой являются более предпочтительными, то энергетически выгодно, чтобы эта часть молекулы контактировала с водой, а ее неполярная область была исключена из такого контакта. Концентрация, при которой 50°/о детергента находятся в составе мицелл, называется критической концентрацией мицеллообразования. С практической точки зрения удобнее определять ККМ как концентрацию, при которой начинают образовываться мицеллы. ККМ соответствует пределу растворимости молекул в мономерном состоянии. Дальнейшее добавление додецилсульфата приводит к увеличению концентрации мицелл.
Липидные агрегаты или мицеллы могут иметь разные размеры и форму. Так, додецилсульфат образует в воде сферические мицеллы, содержащие около 60 молекул на мицеллу. Некоторые детергенты и амфифильные молекулы могут образовывать как глобулярные, так и цилиндрические агрегаты. Фосфолипиды спонтанно агрегируют с образованием бислоев, которые по сути представляют собой своеобразную разновидность мицелл. Причины, по которым природные фосфолипиды образуют стабильные бислои, будут рассмотрены в следующем разделе. А здесь мы проведем количественный анализ связи между гидрофобностью и ККМ.
Водный раствор амфифильного соединения может состоять из смеси разных форм, включая мономеры и различные агрегаты из большого числа молекул. В равновесии химический потенциал амфифильного соединения в каждой из форм будет одинаковым:
кТ= ftv + jy\n = Константа, одинаковая для всех N,
где fiN - стандартный химический потенциал агрегатов, содержащих N молекул, Х\ - мольная доля амфифильных молекул в агрегатах, содержащих N молекул, к - константа Больцмана, Т - температура. Для простоты рассмотрим монодисперсную систему с М молекулами на один агрегат. Это означает, что есть только один тип агрегатов с N = М, находящихся в равновесии с мономером. Хотя это и явное упрощение, но оно вполне приемлемо для молекул, образующих сферические мицеллы или небольшие моноламел-лярные везикулы. Теперь рассмотрим условия равновесия системы при критической концентрации мицеллообразования и представим ККМ как такую концентрацию, при которой Х\ = Хм:
Другие статьи:
Результаты исследований и их обсуждение
Территория исследуемого школьного участка (3,7 га) находится по адресу: с. Айкино, ул. Центральная, д. 100 «А». Она покрыта растительностью на площади в 3,3 га. В отличие от естественных сообществ, антропогенные ландшафты характеризуются ...
Рост мозга. Развитие коры головного мозга. Развитие
интеллекта. Эмоциональное развитие. Функциональные блоки мозга
Дифференциация систем мозговой коры происходит постепенно, и это приводит к неравномерному созреванию отдельных мозговых структур, входящих в три функциональных блока мозга. При рождении у ребенка практически полностью сформированы подкор ...
Традиции и решения
проблемы разума
Важно проследить (и обобщить) в учениях о разуме тенденцию активности разума познающего и действующего субъекта. У Канта это способность продуктивного воображения; у Фихте акцент на субъективности действующего “я", на волевой активно ...
