Структура фотосинтетических реакционных центров ft. viridis и ft.
sphaeroidesСтраница 2
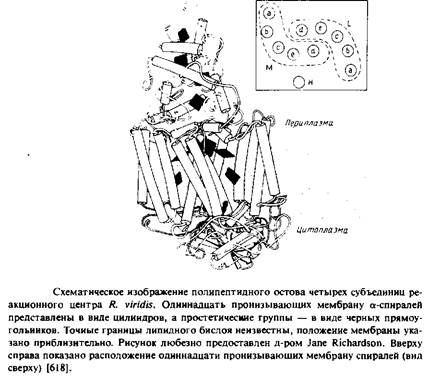
Эти межмолекулярные взаимодействия в кристаллах осуществляются между участками Н-субъединицы и цитохромом, которые в норме контактируют с водой. Возможно, эти два белка, образующие гидрофильные "шапочки", способствуют формированию высокоупорядоченных кристаллов.
Отметим некоторые важные структурные особенности рассматриваемого комплекса.
Все 11 трансмембранных участков представляют собой а-спирали, а составляющие их аминокислоты в большинстве своем неполярны. В каждой из трансмембранных спиралей L-и М-субъединиц имеется последовательность длиной не менее 19 остатков, не содержащая никаких кислых или основных аминокислот.
Трансмембранные спирали в каждой из субъединиц L или М обычно антипараллельны своим соседям, но спирали сие параллельны друг другу. Наклон спиралей к нормали к плоскости мембраны не превышает 25°, за исключением спирали d, которая наклонена к нормали под углом 38°. Длина спиралей варьирует от 24 до 30 остатков.
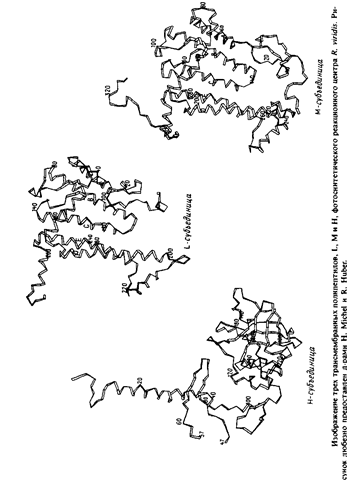
Те участки L - и М-субъединиц, которые соединяют трансмембранные сегменты, образуют уплощенные структуры по обе стороны мембраны, которые могут контактировать с двумя гидрофильными субъединицами.
Заряженные аминокислоты в субъединицах L и М распределены асимметрично, так что полярные концы трансмембранных спиралей и соединяющие их участки заряжены более отрицательно на периплазматической стороне мембраны, чем на цитоплазматической. Это создает определенные энергетические выгоды, поскольку мембранный потенциал отрицателен на цитоплазматической стороне.
Все эти структурные данные ценны также в том отношении, что они помогают понять фотохимию этого важного комплекса.
Хотя редокс-центры, по-видимому, создают два параллельных пути переноса электронов от "специальной пары", эти две ветви не идентичны, и при переносе электронов через мембрану, вероятно, используется только одна из них. Фотосинтетические пигменты жестко фиксируются в определенном месте за счет гидрофобных взаимодействий и водородных связей с белком и вряд ли перемещаются во время реакции.
Перенос электрона от "специальной пары" к бактериофеофитину происходит очень быстро; это согласуется с тем, что участвующие в процессе простетические группы находятся друг от друга на расстоянии вандерваальсового радиуса. Характерное время переноса электрона от бактериофеофитина к Qa составляет 230 пс, и центры этих двух групп разделены расстоянием около 14 А. Однако изопреноидная боковая цепь хинона непосредственно контактирует с бактериофеофитином.
Перенос электрона от цитохрома, сопровождающийся восстановлением специальной пары, происходит медленно, за 270 не, в соответствии с тем, что центр ближайшего гема расположен от центра специальной пары на расстоянии 21 А. Из-за этого, в частности, замедляется перенос электрона.
Перенос QA Qb может осуществляться при участии негемового железа, хотя оно, по-видимому, не является необходимым для этого процесса. Хинон Qb связывается слабо и утрачивается в процессе приготовления образца. Возможно, функциональная роль Н-субъединицы состоит в связывании QB.
Другие статьи:
Некоторые простые модели движения мембранных
компонентов
На рис. 2 представлены некоторые модели, использующиеся для анализа поступательного движения молекул внутри мембранного бислоя. Такие модели необходимы для интерпретации экспериментальных данных с точки зрения молекулярного движения.
М ...
В.И. Вернадский "О биосфере и живом веществе"
В трудах В. И. Вернадского можно встретить различные определения понятия "биосфера", и , как считает академик Б. С. Соколов, ученый не дал (не ставил своей целью) какого-либо энциклопедически точного определения. Он как бы раскр ...
Позвоночный столб
Позвоночный столб (позвоночник), columna vertebralis, образован последовательно накладывающимися друг на друга позвонками, которые соединены между собой при помощи межпозвоночных дисков, связок и суставов. Формируя осевой скелет, позвоноч ...
